Linfoma
Linfoma es un término general que engloba 40 tipos distintos de cáncer, todos generados a partir de las células blancas de la sangre conocidas como linfocitos. El linfoma se divide habitualmente en dos tipos: linfoma de Hodgkin y de no-Hodgkin, representando este último el 80% de los casos.ANCHOR
Patología
Trasplantes de células madre
Anticuerpos
Vacunas
Referencias
Patología
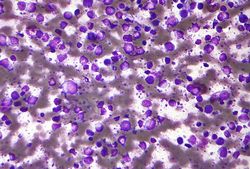 Tanto los linfomas de Hodgkin como de no-Hodgkin son causados por células blancas cancerígenas en los nodos linfáticos. Los dos tipos se diferencian únicamente al observar las células de los nodos linfáticos bajo el microscopio, dado que cada uno afecta a un tipo distinto de células blancas. El linfoma de Hodgkin puede distinguirse por la presencia de células Reed-Sternberg.
Tanto los linfomas de Hodgkin como de no-Hodgkin son causados por células blancas cancerígenas en los nodos linfáticos. Los dos tipos se diferencian únicamente al observar las células de los nodos linfáticos bajo el microscopio, dado que cada uno afecta a un tipo distinto de células blancas. El linfoma de Hodgkin puede distinguirse por la presencia de células Reed-Sternberg.
El linfoma de Hodgkin afecta habitualmente a personas jóvenes (de 15-40 años de edad) y en la edad adulta tardía (más de 55 años de edad).ANCHOR Mientras el linfoma No-Hodgkin se diagnostica en adultos de más de 65, es también la forma más frecuente de cáncer en niños.ANCHOR
Las tasas de supervivencia varían significativamente dependiendo del tipo y estadio de la enfermedad, así como de la edad del paciente. Sin embargo, en las últimas tres décadas las tasas han aumentado significativamente.ANCHOR ANCHOR Los tratamientos estándares son la radioterapia y/o la quimioterapia, pero en los últimos años se han hecho numerosos avances.
Trasplantes de células madre
La quimioterapia y la radioterapia se usan a menudo para destruir las células blancas de la sangre. No obstante, también matan las células activas del sistema inmune, además de las células madre que pueden producir más de estas. Para arreglar este problema una vez concluido el tratamiento, los pacientes pueden recibir un trasplante de células madre hematopoyéticas que se encuentran en la médula ósea.
Tan recientemente como en los años setenta, se creía que los trasplantes de médula eran imposibles.ANCHOR Todos los intentos producían la muerte causada por infecciones o por reacciones inmunes. Este fue un resultado inesperado tras ensayos exitosos con roedores y, sin embargo, ello podría haberse debido a la naturaleza innata de los especímenes de laboratorio.
Don Thomas, que ganó el Nobel Prize en 1990 por su trabajo, realizó experimentos con perros, dotados de una variación genética similar a la de los humanos y que pueden desarrollar enfermedades de la sangre como el linfoma no-Hodgkin.ANCHOR Ingenió un procedimiento basado en la radiación para destruir el cáncer, compatibilizando el tejido entre el donante y el recipiente, y cócteles de fármacos para inhibir el sistema inmunitario. A pesar de que las tasas iniciales de supervivencia eran bajas, el progreso gradual de los fármacos anti-rechazo permitieron el trasplante de donantes sin vínculos de sangre en 1979.
Recientemente se ha visto que el Meloxicam, un fármaco similar a la aspirina, fomenta que las células madre abandonen la médula ósea después de una trasplante, lo cual puede resultar un problema excepcional en el linfoma no-Hodgkin.ANCHOR Esto se puso a prueba primero en ratones y luego en babuinos antes de que ahora se esté probando en ensayos con humanos.
Anticuerpos
Para evitar la destrucción de células madre hematopyéticas pueden usarse anticuerpos monoclonales para alterar específicamente a los linfocitos, células blancas de la sangre, incluidas las células malignas que causan el linfoma. Los anticuerpos reconocen estas células y se encierran dentro de éstas, lo que da como resultado que el sistema inmunitario destruya la célula. El Campath 1-H, o alemtuzumab, és un anticuerpo de rata humanizado, que se usó por primera vez en 1988 para tratar el linfoma no-Hodgkin.ANCHOR ANCHOR El anticuerpo de rata inicial fue rechazado por el sistema inmunitario y se destruyó a si mismo, pero a través de técnicas de ingeniería genética, los investigadores tomaron las regiones importantes para el reconocimiento del anticuerpo de rata y lo colocaron en el interior del gen que codifica el anticuerpo humano. Este abordaje innovador se ha aplicado desde entonces a otros cánceres, y el Campath en sí mismo se está investigando como posible tratamiento para la esclerosis múltiple.ANCHOR ANCHOR
El Rixutan, o rituximab, es ahora uno de los tratamientos estándar para el linfoma y se basa en el mismo principio que el Campath.ANCHOR Es un anticuerpo quimérico ratón/humano y a menudo se usa en combinación con un tratamiento de quimioterapia conocido como CHOP (ciclofosfamida, hidroxidaunorrubicina, oncovina, prednisona). También se usa en tratamientos para leucemia linfocítica crónica y en la artritis reumatoide.ANCHOR
Los anticuerpos se han usado también para dirigir fuentes de radiación a células cancerígenas y apuntarlas así con mayor eficiencia.ANCHOR Tanto la Zevalina (ibritumonab tiuxetan) como Bexxar (tositumomab) fueron fármacos pioneros aprobados a principios de este siglo.ANCHOR Estos fármacos se formaron a partir de isotopos radiactivos ligados a los anticuerpos de ratón que reconocen y se adhieren a las células cancerígenas. Se trata de tratamientos muy potentes que resultan incluso efectivos en cánceres resistentes al Rituxan.
Vacunas
Unlike most vaccines that aim to prevent a disease, a lymphoma vaccine aims to stimulate the immune system into attacking the cancerous cells that are already present.ANCHOR Se han hecho algunos ensayos de vacunas que no han resultado lo suficientemente efectivas. No obstante, una nueva vacuna llamada BiovaxID ha mostrado resultados prometedores en los ensayos clínicos en fase III en el 2010.ANCHOR Las vacunas se manufacturan para dirigirse (apuntar a) cierta proteína en la superfície de las células cancerígenas, conocida como idiotipo. En la actualidad, es necesario que cada vacuna se diseñe a medida del cáncer de cada paciente. Esto puede llevar varios meses y resulta muy caro, de modo que se sigue investigando para encontrar una diana genérica para todos los linfomas.
La vacuna se dirige actualmente a atacar el linfoma folicular, la forma más frecuente de linfoma de bajo grado. El cáncer tiende a cursar en ciclos de remisión y recaída a medida que desarrolla resistencia a distintos tratamientos. La vacuna está diseñada para ser usada a estadíos tempranos o cuando el cáncer se encuentra en fase de remisión para destruir las células restantes. Este abordaje aumenta el tiempo entre remisiones de 30 a 44 meses.
En el año 2012, la FDA aseguró que no aprobaría la vacuna para usarse en los EEUU sin que se hicieran más ensayos, lo que llevó a la bancarota al fabricante.ANCHOR No obstante, todavia se espera que la vacuna alcance la aprobación en el mercado Europeo y de Canadá a finales del 2014.
Referencias
- http://www.canceractive.com/cancer-active-page-link.aspx?n=164
- http://www.cancerresearchuk.org/cancer-info/cancerstats/types/hodgkinslymphoma/
- http://www.cancerresearchuk.org/cancer-info/cancerstats/types/nhl/
- http://www.cancerresearchuk.org/cancer-info/cancerstats/types/nhl/
- http://www.cancerresearchuk.org/cancer-info/cancerstats/types/hodgkinslymphoma/
- http://www.nature.com/nature/journal/v491/n7424/full/491334a.html
- http://www.nature.com/nature/journal/v491/n7424/full/491334a.html
- Hoggatt J et al (2013) Differential stem- and progenitor-cell trafficking by prostaglandin E2 Nature 495:365–369 doi:10.1038/nature11929
- http://www.newscientist.com/article/mg13318103.700-technology-human-antibody-goes-on-trial.html
- Riechmann L, Clark M, Waldmann H, Winter G. (1988) Reshaping human antibodies for therapy. Nature 332:323-7 doi:10.1038/332323a0
- Cohen JA et al (2012) Alemtuzumab versus interferon beta 1a as first-line treatment for patients with relapsing-remitting multiple sclerosis: a randomised controlled phase 3 trial The Lancet 380(9856):1819-1828 doi:10.1016/S0140-6736(12)61769-3
- Coles AJ et al (2012) Alemtuzumab for patients with relapsing multiple sclerosis after disease-modifying therapy: a randomised controlled phase 3 trial The Lancet 380(9856):1829-1839 doi:10.1016/S0140-6736(12)61768-1
- Scott SD (1998) Rituximab: a new therapeutic monoclonal antibody for non-Hodgkin's lymphoma Cancer Pract 6(3): 195–7. doi:10.1046/j.1523-5394.1998.006003195.x
- Saini KS et al (2011) Rituximab in Hodgkin lymphoma: Is the target always a hit? Cancer Treat Rev 37 (5): 385–90 doi:10.1016/j.ctrv.2010.11.005
- Milenic DE, Brady ED and Brechbiel MW (2004) Antibody-targeted radiation cancer therapy Nature Rev Drug Discovery 3:488-98 doi:10.1038/nrd1413
- Rao AV, Akabani G and Rizzieri DA (2005) Radioimmunotherapy for Non-Hodgkin's Lymphoma Clin Med Res 3(3):157-65 doi:10.3121/cmr.3.3.157
- Lee ST et al (2007) BiovaxID: a personalized therapeutic cancer vaccine for non-Hodgkin's lymphoma Expert Opin Biol Ther 7(1):113-22 doi:10.1517/14712598.7.1.113
- Schuster SJ et al (2011) Vaccination With Patient-Specific Tumor-Derived Antigen in First Remission Improves Disease-Free Survival in Follicular Lymphoma Journal of Clinical Oncology 29 doi: 10.1200/JCO.2010.33.3005
- http://www.fiercevaccines.com/story/biovest-bankruptcy-shows-travails-cancer-vaccine-development/2013-03-13
Last edited: 17 September 2014 16:21
